Глюкагон – пептидний гормон, що виробляється альфа-клітинами підшлункової залози. Глюкагон підвищує концентрацію глюкози та жирних кислот у крові, і вважається головним катаболічним гормоном організму. Глюкагон також використовується як ліки для лікування ряду захворювань. Ефект глюкагону протилежний ефекту інсуліну, який знижує позаклітинну глюкозу. Глюкагон виробляється з проглюкагону, кодованого геном GCG.
Підшлункова залоза виділяє глюкагон, коли кількість глюкози в крові занадто низька. Глюкагон змушує печінку брати участь у глікогенолізі: перетворюючи накопичений глікоген у глюкозу, яка виділяється в кров. З іншого боку, високий рівень глюкози в крові стимулює вивільнення інсуліну. Інсулін дозволяє засвоювати і використовувати глюкозу інсулінозалежними тканинами. Таким чином, глюкагон та інсулін є частиною системи зворотного зв’язку, яка підтримує стабільний рівень глюкози в крові. Глюкагон збільшує витрати енергії і підвищується в умовах стресу. Глюкагон належить до сімейства секретинів гормонів.
Функція глюкагону
Глюкагон, як правило, підвищує концентрацію глюкози в крові, сприяючи глюконеогенезу та глікогенолізу. Глюкагон також зменшує синтез жирних кислот у жировій тканині та печінці. Глюкагон сприяє ліполізу в цих тканинах, що змушує їх виділяти жирові кислоти в циркуляцію, де вони можуть катаболізуватися, виробляючи енергію в таких тканинах, як скелетні м’язи, коли це потрібно.
Глюкоза зберігається в печінці у вигляді полісахаридного глікогену, який є глюканом (полімером, що складається з молекул глюкози). Клітини печінки (гепатоцити) мають рецептори глюкагону. Коли глюкагон зв’язується з рецепторами глюкагону, клітини печінки перетворюють глікоген в окремі молекули глюкози і виділяють їх у кров, в процесі, відомому як глікогеноліз. Коли запаси глюкози виснажуються, глюкагон спонукає печінку та нирки синтезувати додаткову глюкозу шляхом глюконеогенезу. Глюкагон вимикає гліколіз у печінці, внаслідок чого проміжні проміжні речовини гліколітичного типу переносяться на глюконеогенез.
Глюкагон також регулює швидкість вироблення глюкози за допомогою ліполізу. Глюкагон викликає ліполіз у людей в умовах придушення інсуліну (наприклад, цукровий діабет 1 типу).
Виробництво глюкагону, як видається, залежить від центральної нервової системи через шляхи, які ще не визначено. Як повідомляється, у безхребетних тварин видалення очних глаз впливає на вироблення глюкагону. Вирізання очної глазки у молодих раків викликає індуковану глюкагоном гіперглікемію.
Механізм дії глюкагону
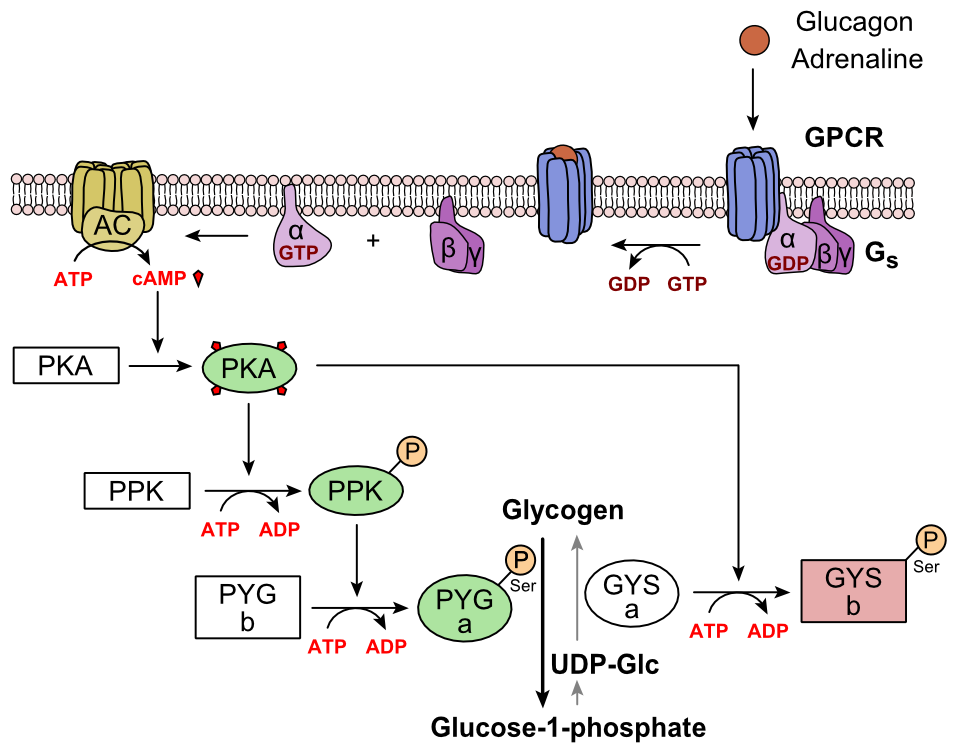
Глюкагон зв’язується з рецептором глюкагону, зв’язаним з білком G рецептором, що знаходиться в плазматичній мембрані клітини. Зміна конформації рецептора активує білки G, гетеротримерний білок з α, β та γ субодиницями. Коли білок G взаємодіє з рецептором, він зазнає конформаційних змін, що призводить до заміщення молекули ВВП, зв’язаної з α-субодиницею, молекулою GTP. Ця заміна призводить до вивільнення α-субодиниці з β та γ-субодиниць. Альфа-субодиниця спеціально активує наступний фермент у каскаді – аденилатциклазу.
Аденилатциклаза виробляє циклічний аденозинмонофосфат (циклічний АМФ або цАМФ), який активує протеїнкіназу А (цАМФ-залежну протеїнкіназу). Цей фермент, у свою чергу, активує фосфорилазакіназу, яка потім фосфорилює глікогенфосфорилазу b (PYG b), перетворюючи її в активну форму, звану фосфорилазою a (PYG a). Фосфорилаза а – фермент, відповідальний за вивільнення глюкози 1-фосфату з полімерів глікогену.
Прикладом шляху може бути, коли глюкагон зв’язується з трансмембранним білком. Трансмембранні білки взаємодіють з Gɑβ𝛾. Gɑ відокремлюється від Gβ𝛾 і взаємодіє з трансмембранним білком аденилілциклазою. Аденилилциклаза каталізує перетворення АТФ в цАМФ. цАМФ зв’язується з протеїнкіназою А, а складний фосфорилює фосфорилазакіназу. Фосфорильована фосфорилаза кіназа фосфорилює фосфорилазу. Фосфорильована фосфорилаза відсікає одиниці глюкози від глікогену у вигляді глюкози 1-фосфату.
Крім того, скоординований контроль гліколізу та глюконеогенезу в печінці регулюється станом фосфорилювання ферментів, що каталізують утворення потужного активатора гліколізу, званого фруктозою 2,6-бісфосфатом. Ензим протеїнкіназа А (РКА), стимульований каскадом, ініційованим глюкагоном, також фосфорилюватиме один сериновий залишок біфункціонального поліпептидного ланцюга, що містить як ферменти фруктоза 2,6-бісфосфатаза, так і фосфофруктокіназа-2. Це ковалентне фосфорилювання, ініційоване глюкагоном, активує перше і інгібує друге. Це регулює реакцію, що каталізує фруктозу 2,6-бісфосфат (потужний активатор фосфофруктокінази-1, ферменту, що є основним регуляторним етапом гліколізу), уповільнюючи швидкість його утворення, тим самим інгібуючи потік шляху гліколізу і дозволяючи глюконеогенез переважати. Цей процес оборотний за відсутності глюкагону (і, отже, присутності інсуліну).
Глюкагонова стимуляція РКА також інактивує гліколітичний фермент піруваткіназу в гепатоцитах.
Фізіологія
Виробництво глюкагону
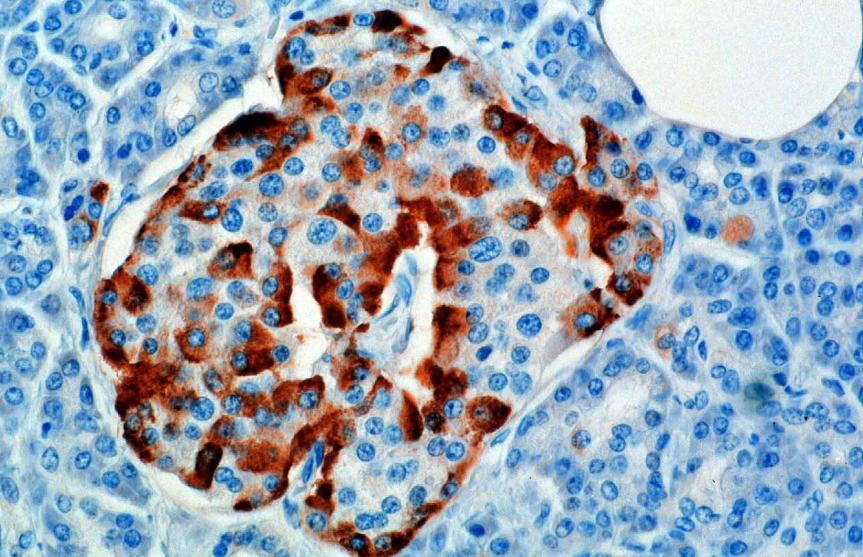
Гормон синтезується і секретується з альфа-клітин (α-клітин) острівців Лангерганса, які розташовані в ендокринній частині підшлункової залози. Виробництво, яке в іншому випадку відбувається вільно, пригнічується / регулюється аміліном – пептидним гормоном, який секретується разом з інсуліном з β-клітин підшлункової залози. Оскільки рівень глюкози в плазмі крові знижується, подальше зниження секреції аміліну полегшує його пригнічення α-клітин, дозволяючи секрецію глюкагону.
У гризунів альфа-клітини розташовані у зовнішньому краю острова. Структура людських острівців набагато менш відокремлена, і альфа-клітини розподіляються по всьому острівці в безпосередній близькості від бета-клітин. Глюкагон також виробляється альфа-клітинами шлунка.
Недавні дослідження показали, що вироблення глюкагону може також відбуватися поза підшлунковою залозою, причому кишечник є найбільш вірогідним місцем синтезу позапанкреатичного глюкагону.
Регулювання глюкагону
Секреція глюкагону стимулюється:
- Гіпоглікемія
- Адреналін (через β2, α2 та α1 адренергічні рецептори)
- Аргінін
- Аланін (часто з трансамінування пірувату / глутамату, отриманого з м’язів
- Ацетилхолін
- Холецистокінін
- Шлунковий інгібуючий поліпептид
Секреція глюкагону пригнічується:
- Соматостатин
- Амілін
- Інсулін (через ГАМК)
- Гетеродимер PPARγ / ретиноїд X-рецептора.
- Підвищений вміст вільних жирних кислот і кетокислот у кров.
- Збільшення виробництва карбаміду
- Глюкагоноподібний пептид-1
Структура глюкагону
Глюкагон – це 29-амінокислотний поліпептид. Його основна структура у людини: NH2-His-Ser-Gln-Gly-Thr-Phe-Thr-Ser-Asp-Tyr-Ser-Lys-Tyr-Leu-Asp-Ser-Arg-Arg-Ala-Gln-Asp-Phe-Val-Gln-Trp -Leu-Met-Asn-Thr-COOH.
Поліпептид має молекулярну масу 3485 дальтон. Глюкагон – пептидний (нестероїдний) гормон.
Глюкагон утворюється в результаті розщеплення проглукагону пропротеїновою конвертазою 2 в клітинах α-острівців підшлункової залози. У кишкових L-клітинах проглюкагон розщеплюється до альтернативних продуктів – гліцентину, GLP-1 (інкретин), IP-2 та GLP-2 (сприяє росту кишечника).
Патологія
Аномально підвищений рівень глюкагону може бути спричинений пухлинами підшлункової залози, такими як глюкагонома, симптоми якої включають некролітичну мігруючу еритему, знижені амінокислоти та гіперглікемію. Це може відбуватися окремо або в контексті множинної ендокринної неоплазії 1 типу.
Підвищений рівень глюкагону є основним фактором, що сприяє гіперглікемічному кетоацидозу при недіагностованому або погано лікуваному діабеті 1 типу. Оскільки бета-клітини перестають функціонувати, інсулін та ГАМК підшлункової залози більше відсутні для придушення вільного виходу глюкагону. В результаті глюкагон вивільняється з альфа-клітин максимум, викликаючи швидкий розпад глікогену до глюкози та швидкий кетогенез. Було виявлено, що підмножині дорослих з діабетом 1 типу в середньому потрібно 4 рази довше, щоб наблизитися до кетоацидозу, якщо їм вводити соматостатин (пригнічує вироблення глюкагону) без інсуліну. Інгібування глюкагону було популярною ідеєю лікування діабету, однак, деякі попереджали, що це призведе до крихкого діабету у пацієнтів з адекватно стабільною глюкозою в крові.
Вважається, що відсутність альфа-клітин (а отже, і глюкагону) є одним з основних впливів на надзвичайну мінливість глюкози в крові при загальній панкреатектомії.
Історія
У 1920-х роках Кімбол і Мурлін вивчали екстракти підшлункової залози і знайшли додаткову речовину з гіперглікемічними властивостями. Вони описали глюкагон у 1923 році. Амінокислотна послідовність глюкагону була описана наприкінці 1950-х. Повніше розуміння його ролі у фізіології та захворюваннях було встановлено лише в 1970-х роках, коли було розроблено специфічний радіоімунологічний аналіз.
.














Discussion about this post