| Альфа-амілаза | |||||||||
|---|---|---|---|---|---|---|---|---|---|
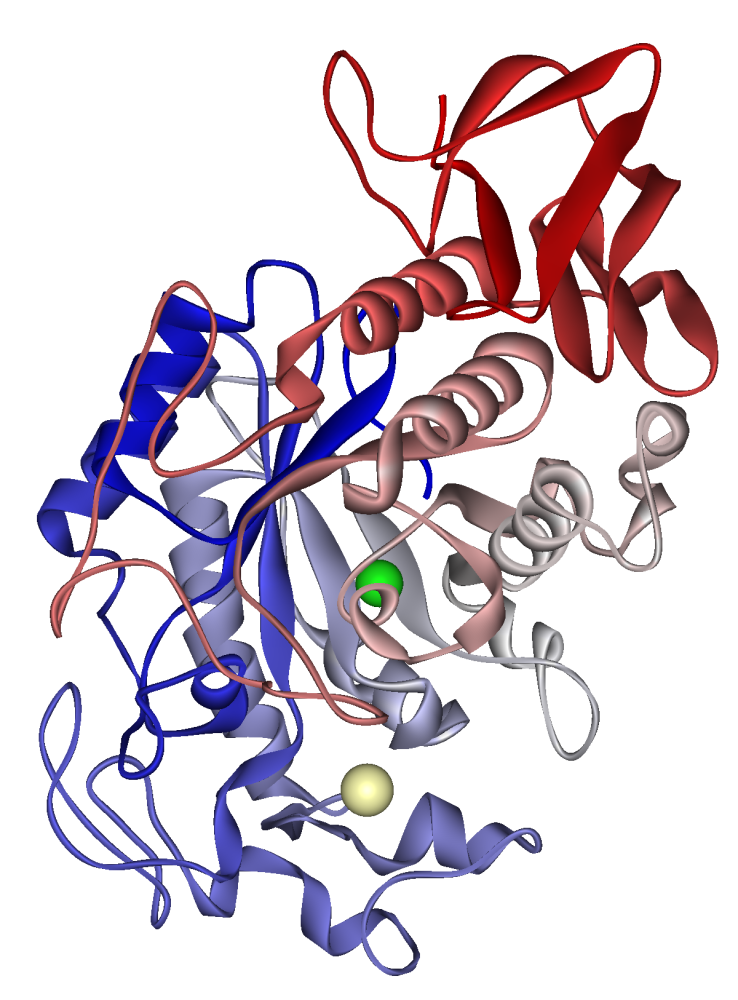
Амілаза слини людини: іон кальцію видно у блідо-хакі, хлорид-іон у зеленому. PDB 1SMD
|
|||||||||
| Ідентифікатори | |||||||||
| № ЄС | 3.2.1.0 | ||||||||
| CAS номер | 9000-90-2 | ||||||||
| Бази даних | |||||||||
| IntEnz | Перегляд IntEnz | ||||||||
| БРЕНДА | Вступ БРЕНДА | ||||||||
| ExPASy | Перегляд NiceZyme | ||||||||
| KEGG | Запис у KEGG | ||||||||
| MetaCyc | метаболічний шлях | ||||||||
| ПРІАМ | профіль | ||||||||
| Структури PDB | RCSB PDB PDBe PDBсума | ||||||||
|
|||||||||
| Каталітичний домен GH13 | |||||||||
|---|---|---|---|---|---|---|---|---|---|

Циклодекстрин глюканотрансфераза (ec2.4.1.19) (cgtase)
|
|||||||||
| Ідентифікатори | |||||||||
| Символ | Альфа-амілаза | ||||||||
| Пфам | PF00128 | ||||||||
| Клан Пфам | CL0058 | ||||||||
| InterPro | IPR006047 | ||||||||
| SCOP2 | 1ppi / SCOPe / SUPFAM | ||||||||
| OPM суперсімейство | 117 | ||||||||
| Білок OPM | 1wza | ||||||||
| CAZy | GH13 | ||||||||
| CDD | cd11338 | ||||||||
|
|||||||||
| Альфа-амілаза С-кінцевий домен бета-аркуша | |||||||||
|---|---|---|---|---|---|---|---|---|---|

Кристалічна структура неактивного мутанта d180a ячменю альфа-амілази ізоферменту 1 (amy1) у комплексі з мальтогептаозою
|
|||||||||
| Ідентифікатори | |||||||||
| Символ | Альфа-аміл_С2 | ||||||||
| Пфам | PF07821 | ||||||||
| InterPro | IPR012850 | ||||||||
|
|||||||||
| Альфа-амілаза, С-кінцевий повністю-бета-домен | |||||||||
|---|---|---|---|---|---|---|---|---|---|
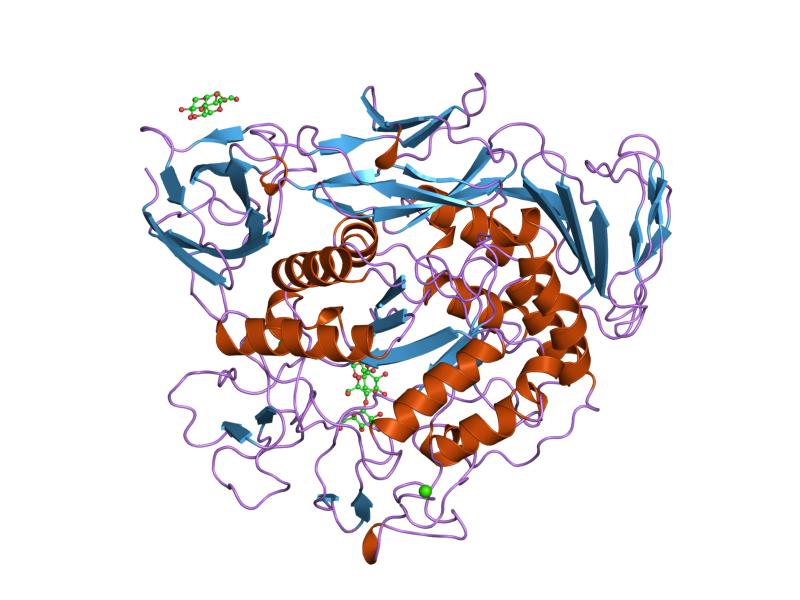
мальтотріозний комплекс попередньо кондиціонованого мутанта циклодекстрину глікозилтрансферази
|
|||||||||
| Ідентифікатори | |||||||||
| Символ | Альфа-амілаза_С | ||||||||
| Пфам | PF02806 | ||||||||
| Клан Пфам | CL0369 | ||||||||
| InterPro | IPR006048 | ||||||||
| SCOP2 | 1ppi / SCOPe / SUPFAM | ||||||||
|
|||||||||
Альфа-амілаза, (α-амілаза) є ферментом EC 3.2.1.1, який гідролізує альфа-зв’язки великих альфа-зв’язаних полісахаридів, таких як крохмаль та глікоген, утворюючи їх коротші ланцюги, декстрини та мальтозу. Це основна форма амілази, що зустрічається у людей та інших ссавців. Він також присутній у насінні, що містить крохмаль як запас їжі, і виділяється багатьма грибами. Він є членом сімейства глікозидгідролази 13.
В біології людини
Незважаючи на те, що амілаза міститься в багатьох тканинах, амілаза є найбільш помітною у соку підшлункової залози та слині, кожна з яких має свою власну ізоформу людської α-амілази. Вони поводяться по-різному при ізоелектричному фокусуванні, і їх також можна розділити під час тестування за допомогою специфічних моноклональних антитіл. У людини всі ізоформи амілази пов’язуються з хромосомою 1p21 (див. AMY1A).
Слинна амілаза (птіалін)
Амілаза міститься в слині і розщеплює крохмаль до мальтози та декстрину. Цю форму амілази також називають “птіалін” /ˈтaɪəlɪn/, яку назвав шведський хімік Йонс Якоб Берцеліус. Назва походить від грецького слова πτυω (я плюю), оскільки речовина була отримана із слини. Він розщепить великі, нерозчинні молекули крохмалю на розчинні крохмалі (амілодекстрин, еритродекстрин та ахродекстрин), утворюючи послідовно менші крохмалі і, врешті-решт, мальтозу. Птіалін діє на лінійні α (1,4) глікозидні зв’язки, але для гідролізу сполук потрібен фермент, який діє на розгалужені продукти. Слинна амілаза інактивується в шлунку шлунковою кислотою. У шлунковому соку, доведеному до рН 3,3, птіалін був повністю інактивований за 20 хвилин при 37 ° С. На відміну від цього, 50% активності амілази залишалося після 150 хвилин впливу шлункового соку при рН 4,3. І крохмаль, і субстрат для птіаліну, і продукт (короткі ланцюги глюкози) здатні частково захистити його від інактивації шлунковою кислотою. Птіалін, доданий до буфера при рН 3,0, зазнав повної інактивації за 120 хвилин; однак додавання крохмалю на рівні 0,1% призвело до того, що 10% активності залишилось, і подібне додавання крохмалю до рівня 1,0% призвело до того, що приблизно 120% активності залишалося на 120 хвилинах.
Оптимальні умови для птіаліну
- Оптимальний рН – 7,0
- Температура тіла людини
- Наявність певних аніонів та активаторів:
- Хлорид і бромід – найбільш ефективні
- Йодид – менш ефективний
- Сульфат і фосфат – найменш ефективні
Генетична варіація амілази слини людини
Ген амілази слини зазнав дублювання під час еволюції, і дослідження гібридизації ДНК показують, що багато людей мають множинні тандемні повтори гена. Кількість копій генів корелює з рівнем амілази в слині, що вимірюється за допомогою аналізів білкової блоттингу з використанням антитіл до амілази людини. Кількість генних копій пов’язана з очевидним еволюційним впливом дієт з високим крохмалем. Наприклад, у японської особини було 14 копій гена амілази (один алель – 10 копій, а другий – чотири копії). Японська дієта традиційно містить велику кількість рисового крохмалю. На відміну від цього, особа Біаки мала шість копій (по три копії на кожному алелі). Біака – це мисливці-збирачі дощових лісів, які традиційно вживають дієту з низьким вмістом крохмалю. Перрі та його колеги припустили, що збільшення кількості копій гена амілази слинної залози могло мати посилене виживання, яке збігається із переходом на крохмалисту дієту під час еволюції людини.
Амілаза підшлункової залози
Α-амілаза підшлункової залози випадковим чином розщеплює α (1-4) глікозидні зв’язки амілози з отриманням декстрину, мальтози або мальтотріози. Він використовує механізм подвійного переміщення із збереженням аномерної конфігурації. У людини амілаза слини еволюціонувала з її копії.
При патології
Тест на амілазу простіший у порівнянні з тестом на ліпазу, що робить його основним тестом, який використовується для виявлення та моніторингу панкреатиту. Медичні лабораторії зазвичай вимірюють або амілазу підшлункової залози, або загальну амілазу. Якщо вимірюється лише амілаза підшлункової залози, збільшення не зафіксується при епідемічному паротиті чи інших травмах слинних залоз.
Однак через невелику кількість часу, час є критичним для забору крові для цього вимірювання. Кров слід брати незабаром після нападу болю при панкреатиті, інакше вона швидко виводиться нирками.
Слинна α-амілаза використовується як біомаркер для стресу та як сурогатний маркер активності симпатичної нервової системи (СНС), який не вимагає забору крові.
Інтерпретація
Підвищений рівень плазми у людини виявляється у:
- Травма слини (включаючи анестезуючу інтубацію)
- Свинка – через запалення слинних залоз
- Панкреатит – через пошкодження клітин, що виробляють амілазу
- Ниркова недостатність – через зменшення виведення
Загальні показники амілази, які в 10 разів перевищують верхню межу норми (ULN), свідчать про наявність панкреатиту. П’ять-десять разів вище норми нормальної норми може свідчити про захворювання клубової кишки, дванадцятипалої кишки або нирок, а нижчі рівні зазвичай спостерігаються при захворюваннях слинних залоз.
Гени
- слинний – AMY1A, AMY1B, AMY1C
- підшлункова – AMY2A, AMY2B
У зерні
Активність α-амілази в зерні вимірюється, наприклад, за допомогою падаючого числа Хагберга – Пертена, тесту для оцінки пошкоджень паростків або методу Фадебаса. Зустрічається в пшениці.
Промислове використання
α-амілаза використовується у виробництві етанолу для розщеплення крохмалів у зернах до ферментованих цукрів.
Першим кроком у виробництві кукурудзяного сиропу з високим вмістом фруктози є обробка кукурудзяного крохмалю α-амілазою, утворюючи більш короткі ланцюги олігосахаридів цукрів.
Α-амілаза під назвою “Термаміл”, похідна з Bacillus licheniformis, також використовується в деяких мийних засобах, особливо в мийних засобах для посуду та крохмалю.
Дивіться амілазу, щоб дізнатися більше про використання сімейства амілаз загалом.
Потенціал для медичного використання
α-амілаза демонструє ефективність при деградації полімікробних бактеріальних біоплівк шляхом гідролізу α (1-4) глікозидних зв’язків у структурних матричних екзополісахаридах позаклітинної полімерної речовини (EPS).
Інгібування буфера
Повідомляється, що молекула трису інгібує ряд бактеріальних α-амілаз, тому їх не слід використовувати в трис-буфері.
Рішучість
Для визначення активності α-амілази доступно кілька методів, і різні галузі, як правило, покладаються на різні методи. Йодний тест на крохмаль, розробка йодного тесту, заснований на зміні кольору, оскільки α-амілаза розкладає крохмаль і зазвичай використовується в багатьох додатках. Подібним, але промислово виробленим тестом є тест на амілазу Фадебас, який використовується як якісний та кількісний тест у багатьох галузях промисловості, таких як миючі засоби, різні борошняні, зернові та солодові продукти, та судова біологія.
Архітектура домену
α-амілази містять ряд різних білкових доменів. Каталітичний домен має структуру, що складається з восьмиланцюгового альфа / бета-бареля, який містить активний центр, перерваний ~ 70-амінокислотним зв’язуючим кальцієм доменом, що виступає між бета-ланцюгом 3 і альфа-спіраллю 3, і карбоксильно-кінцевим грецьким ключовий домен бета-бочки. Кілька альфа-амілаз містять домен бета-листа, як правило, на кінці С. Цей домен організований у вигляді п’ятиланцюгового антипаралельного бета-аркуша. Кілька альфа-амілаз містять повністю бета-домен, як правило, на кінці С.
.















Discussion about this post