Резюме
- Дослідники лікували серповидно-клітинну хворобу на мишах шляхом безпосереднього редагування дефектного гемоглобінового гена, який викликає це захворювання.
- Ці висновки можуть призвести до одноразового лікування серповидноклітинної хвороби з меншою кількістю побічних ефектів, ніж інші методи лікування, що розробляються.
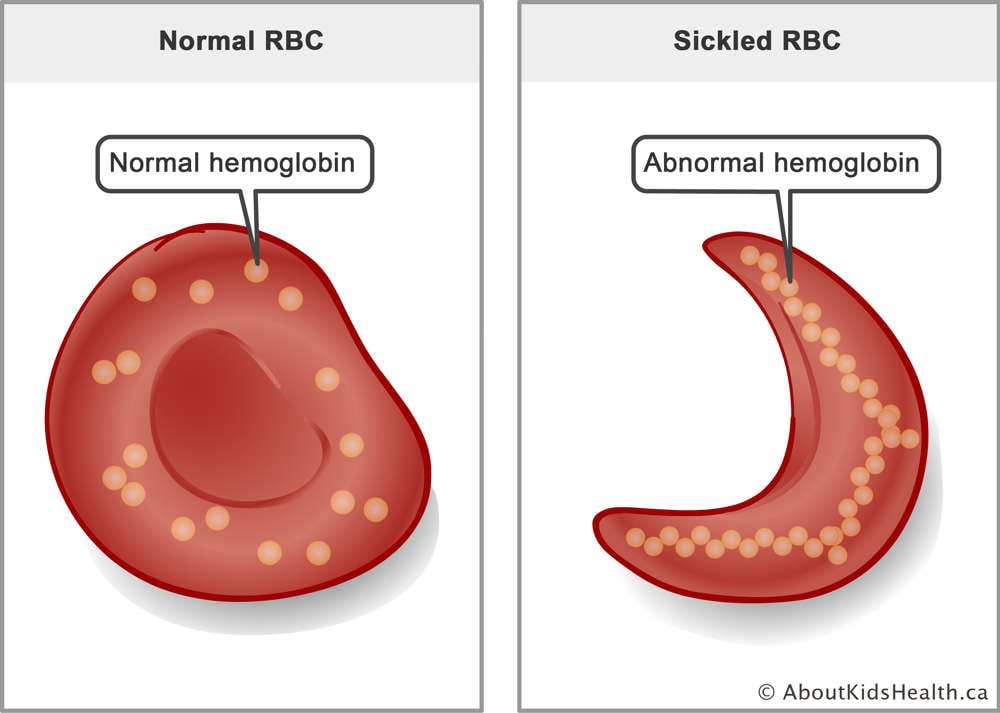
Серповидно-клітинна хвороба (ГКС) – це генетичне захворювання, спричинене мутацією обох копій гена HBB людини. Цей ген кодує компонент гемоглобіну, який є білком, що несе кисень, в еритроцитах. Мутація змушує молекули гемоглобіну злипатися, створюючи серпоподібні еритроцити. Цей процес може призвести до розриву клітин крові, анемії, періодичного болю, імунодефіциту, пошкодження органів та ранньої смерті. Трансплантація кісткового мозку може вилікувати СЦД, але відповідні донори важко знайти. Процедура трансплантації також несе ризик небезпечних побічних ефектів.
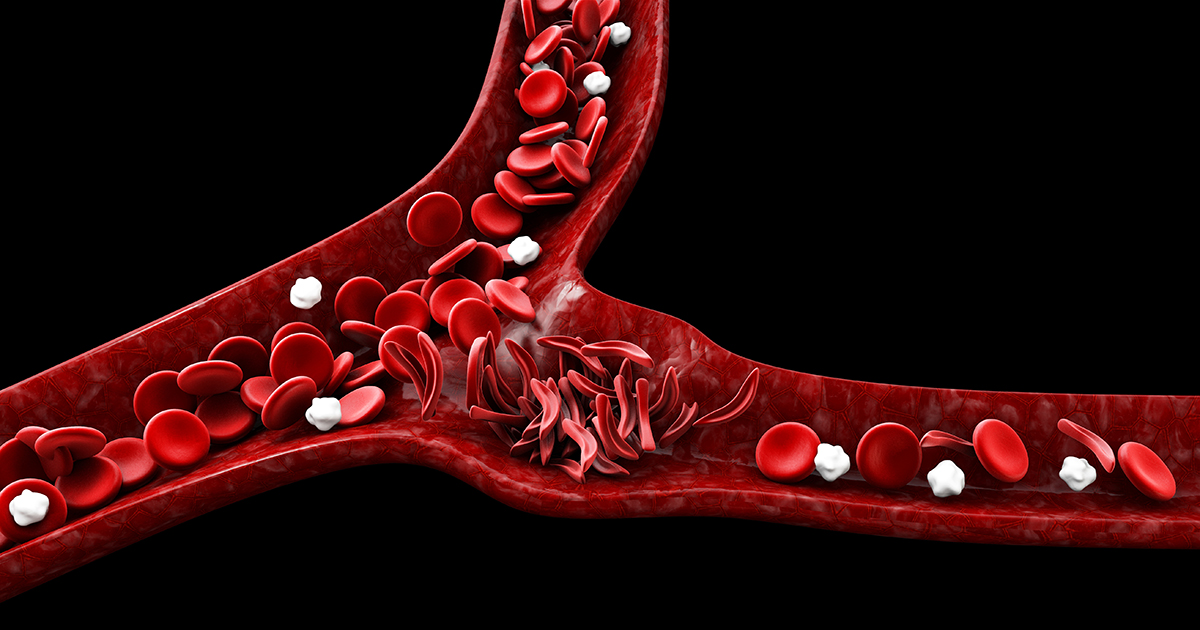
В даний час розробляється кілька нових методів лікування серповидноклітинної хвороби. Ці методи включають редагування генів власних клітин кісткового мозку пацієнта для отримання нормально функціонуючого гемоглобіну. Ці методи лікування дозволяють уникнути ризиків, пов’язаних з трансплантацією кісткового мозку. Але ці методи також несуть власні ризики, оскільки вони включають введення нової ДНК та розщеплення існуючих ниток ДНК.
Група дослідників, яку очолювали доктор Девід Лю з Інституту Броуд та д-р Мітчелл Вайс та д-р Джонатан Єн з дитячої лікарні Сент-Джуд у США, розробили метод, який дозволяє уникнути деяких ризиків інших підходів до редагування генів. Цей метод використовує молекулярну техніку, яка називається редагуванням основи, яка змінює одну букву геному, не вирізаючи жодної ДНК.
При серповидно-клітинній хворобі Т замінює А у ключовій локалізації гена HBB. Хоча базове редагування не може змінити цю зміну, воно може перетворити T на C. Ця дія утворює природний непатогенний варіант гемоглобіну, який називається Hb-Makassar. Дослідники розробили молекулярний інструмент, який називається редактором базису аденина, який розпізнає мутовану частину гена і перетворює Т в С.
Дослідники використовували редактор базису аденіну на кровотворних стовбурових клітинах пацієнтів із ССД людини. До 80% клітин мали геноз серповидноклітинного гемоглобіну, перетворений у варіант Макассара. Для тестування команда пересадила відредаговані клітини людини в мишачу модель SCD. Через 16 тижнів після трансплантації у 68% отриманих донорами стовбурових клітин гени HBB були відредаговані в Hb-Makassar. Еритроцити, отримані з цих стовбурових клітин, значно зменшили серп.
Оскільки червоні кров’яні клітини людини не можуть вижити у мишей досить довго для масштабних випробувань, наступна команда взяла стовбурові клітини з моделі мишачого СЦД, відредагувала їх і пересадила відредаговані клітини в інший набір мишей. Через 16 тижнів варіант Макассара складав майже 80% гемоглобіну у мишей-реципієнтів. У контрольних мишей, які отримували нередаговані клітини, були характерні симптоми СЦД: анемія, ненормальний вміст клітин крові, серпоподібні еритроцити та збільшена селезінка. Миші, які отримували відредаговані стовбурові клітини, мали значно покращені симптоми.
Дослідники взяли кістковий мозок у мишей, які отримали відредаговані стовбурові клітини, і пересадили його на новий набір мишей. Нові реципієнти мали здоровий рівень клітин крові, що підтверджує довговічність редагування гена. Далі дослідники встановили, що редагування принаймні 20% копій генів SCD було достатнім для підтримання здорового рівня крові. Вони не виявили жодних побічних ефектів у мишей у процесі редагування генів.
“Цей підхід пропонує обіцянку як основу одноразового лікування або, можливо, навіть одноразового лікування серповидно-клітинної хвороби”, – говорить Лю.
Зараз команда працює над подальшим розвитком концепції з кінцевою метою охопити пацієнтів.
.














Discussion about this post