Спадковий неполіпозний колоректальний рак (HNPCC), також називається Синдром Лінча, є аутосомно-домінантним генетичним станом, який пов’язаний з високим ризиком раку товстої кишки, а також інших видів раку, включаючи рак ендометрія (другий за частотою), яєчники, шлунок, тонкий кишечник, гепатобіліарний тракт, верхні сечовивідні шляхи, мозок та шкіру. Підвищений ризик цих видів раку обумовлений успадкованими мутаціями, які погіршують відновлення невідповідності ДНК. Це різновид ракового синдрому.
Симптоми синдрому Лінча
Ризик раку
Довічний ризик та середній вік при діагностиці раку, асоційованого із синдромом Лінча
| Тип раку | Довічний ризик (%) | Середній вік на момент встановлення діагнозу (роки) |
| Колоректальний | 52-58 | 44-61 |
| Ендометрій | 25-60 | 48-62 |
| Шлунковий | 6-13 | 56 |
| Яєчники | 4-12 | 42,5 |
На додаток до видів раку, наведених на діаграмі вище, розуміється, що синдром Лінча також сприяє підвищеному ризику розвитку раку тонкої кишки, раку підшлункової залози, раку сечоводу / ниркової миски, раку жовчних шляхів, раку головного мозку та сальних новоутворень. Підвищений ризик раку передміхурової залози та раку молочної залози також був пов’язаний із синдромом Лінча, хоча ця взаємозв’язок до кінця не зрозуміла.
Дві третини раку товстої кишки виникають у проксимальній частині товстої кишки, а загальні ознаки та симптоми включають кров у калі, діарею або запор та ненавмисну втрату ваги. Середній вік діагнозу раку прямої кишки становить 44 роки для членів сімей, які відповідають амстердамським критеріям. Середній вік діагностики раку ендометрія становить близько 46 років. Серед жінок з HNPCC, які страждають на рак товстої кишки та ендометрія, приблизно половина з перших страждає на рак ендометрія, що робить рак ендометрія найпоширенішим дозорним раком при синдромі Лінча. Найпоширенішим симптомом раку ендометрія є аномальна вагінальна кровотеча. У HNPCC середній вік діагнозу раку шлунка становить 56 років, причому аденокарцинома кишкового типу є найбільш поширеною патологією. Рак яєчників, асоційований з HNPCC, має середній вік діагностики 42,5 років; приблизно 30% діагностують до 40 років.
Виявлено значну різницю в швидкості раку в залежності від задіяної мутації. До віку 75 років ризики колоректального раку, раку ендометрія, раку яєчників, верхніх відділів шлунково-кишкового тракту (шлунка, дванадцятипалої кишки, жовчної протоки або підшлункової залози), раку сечовивідних шляхів, раку простати та пухлин головного мозку були такими: для мутацій MLH1 ризик становив 46%, 43%, 10%, 21%, 8%, 17% та 1% відповідно; для мутацій MSH2 ризики становили 57%, 17%, 10%, 25%, 32% та 5% відповідно; для мутацій MSH6 ризики становили 15%, 46%, 13%, 7%, 11%, 18% та 1% відповідно.
| Ген | Ризик раку яєчників | Ризик раку ендометрія |
|---|---|---|
| MLH1 | 4-24% | 25-60% |
| MSH2 / EPCAM | 4-24% | 25-60% |
| MSH6 | 1-11% | 16-26% |
| PMS2 | 6% (сукупний ризик) | 15% |
Генетика

HNPCC успадковується автосомно-домінантно. Відмітною ознакою HNPCC є дефектне відновлення невідповідності ДНК, що спричиняє підвищену швидкість змін одиничних нуклеотидів та нестабільність мікросупутника, також відому як MSI-H (H “висока”). MSI можна ідентифікувати в зразках раку в лабораторії патології. Більшість випадків призводять до зміни тривалості повторів динуклеотидів нуклеобаз цитозину та аденину (послідовність: CACACACACA…).
4 основні гени, що беруть участь у HNPCC, зазвичай кодують функціонування білків, що утворюють димери:
- Білок MLH1 димеризується з білком PMS2, утворюючи MutLα, який координує зв’язування інших білків, що беруть участь у відновленні невідповідностей, таких як ДНК-геліказа, одноланцюговий білок, що зв’язує ДНК (RPA), і ДНК-полімерази.
- Білок MSH2 димеризується з білком MSH6, який визначає невідповідність за допомогою моделі ковзного затиску, білка для сканування на наявність помилок.
Порушення будь-якого гена білкового димеру погіршує функцію білка. Ці 4 гени беруть участь у виправленні помилок (виправлення невідповідностей), тому дисфункція генів може призвести до нездатності виправити помилки реплікації ДНК та спричинити HNPCC. Відомо, що HNPCC асоціюється з іншими мутаціями генів, що беруть участь у шляху відновлення невідповідності ДНК:
| Ім’я OMIM | Гени, причетні до HNPCC | Частота мутацій у сім’ях HNPCC | Локус | Перша публікація |
|---|---|---|---|---|
| HNPCC1 (120435) | MSH2 / EPCAM | приблизно 60% | 2р22 | Фішель 1993 |
| HNPCC2 (609310) | MLH1 | приблизно 30% | 3p21 | Пападопулос 1994 |
| HNPCC5 | MSH6 | 7-10% | 2р16 | Міякі 1997 |
| HNPCC4 | PMS2 | відносно нечасто | 7р22 | Ніколаїдес 1994 |
| HNPCC3 | ПМС1 | повідомлення про справу | 2q31-q33 | Ніколаїдес 1994 |
| HNPCC6 | TGFBR2 | повідомлення про справу | 3р22 | |
| HNPCC7 | MLH3 | спірний | 14q24.3 |
Більшість людей з HNPCC успадковують цей стан від батьків. Однак через неповну пенетрантність, мінливий вік діагностики раку, зменшення ризику раку або ранню смерть не всі люди з мутацією гена HNPCC мають батьків, які мали рак. Деякі люди розвивають HNPCC de-novo у новому поколінні, не успадковуючи ген. Ці люди часто ідентифікуються лише після розвитку раку товстої кишки у ранньому віці. Батьки з HNPCC мають 50% шансів передати генетичну мутацію кожній дитині. Важливо також зазначити, що шкідливої мутації одного з генів MMR недостатньо для того, щоб викликати рак, але, швидше за все, мають відбуватися подальші мутації в інших генах-супресорах пухлини.
Діагностика синдрому Лінча
Діагноз синдрому Лінча застосовують до людей із мутацією ДНК зародкової лінії в одному з генів MMR (MLH1, MSH2, MSH6 та PMS2) або гені EPCAM, виявлених генетичним тестуванням. Кандидатів на генетичне тестування на зародкові лінії можна визначити за клінічними критеріями, такими як Амстердамські клінічні критерії та Рекомендації Бетесди, або за допомогою аналізу пухлини за допомогою імуногістохімії (IHC) або тестування на мікросателітну нестабільність (MSI). У США професійні товариства рекомендують тестувати кожен рак товстої кишки на MSI або IHC як скринінг на синдром Лінча, але це не завжди проводиться через обмеження витрат та ресурсів. Генетичне тестування комерційно доступне і складається з аналізу крові.
Імуногістохімія
Імуногістохімія (IHC) – метод, який може бути використаний для виявлення експресії білка з відхиленням від норми невідповідності (MMR) у пухлинах, які пов’язані із синдромом Лінча. Хоча це не є діагностикою синдрому Лінча, він може зіграти певну роль у визначенні людей, яким слід пройти тестування на зародкові лінії. Два методи впровадження IHC тестування включають вікове та універсальне тестування для всіх людей. В даний час не існує загальної згоди щодо того, який метод скринінгу слід використовувати. Частково пропонується вікове тестування на IHC завдяки аналізу витрат та вигод, тоді як універсальне тестування для всіх людей, які страждають на рак прямої кишки, гарантує, що люди з синдромом Лінча не пропускаються. Для покриття витрат дослідники намагаються передбачити MSI або IHC безпосередньо з того, як пухлина виглядає під мікроскопом, не проводячи молекулярних досліджень.
Нестабільність мікросупутника
Мутації в системах відновлення невідповідностей ДНК можуть призвести до труднощів передачі ділянок всередині ДНК, які містять повторювані структури двох або трьох нуклеотидів (мікросателітів), інакше відомих як нестабільність мікросателітів (MSI). MSI ідентифікується шляхом вилучення ДНК як із зразка тканини пухлини, так і з нормального зразка тканини з подальшим ПЛР-аналізом мікросателітних областей. Аналіз MSI може бути використаний для виявлення людей, які можуть мати синдром Лінча, та направлення їх на подальше тестування.
Класифікація
Три основні групи раку MSI-H (мікросупутникова нестабільність – MSI) можна розпізнати за гістопатологічними критеріями:
- правобічний малодиференційований рак
- правобічний муцинозний рак
- аденокарциноми в будь-якому місці, що демонструє будь-який вимірюваний рівень інтраепітеліального лімфоциту (ТІЛ)
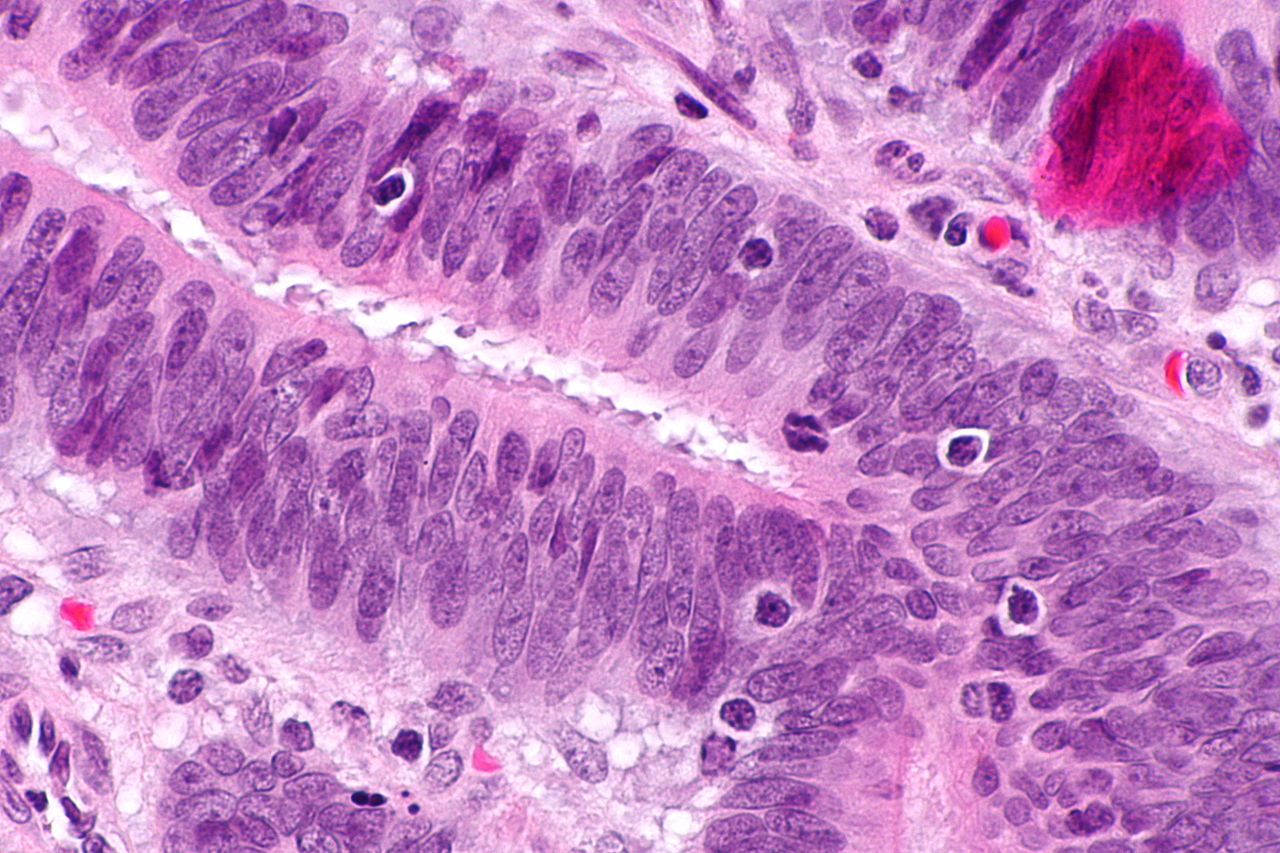
Гістопатологічні критерії недостатньо чутливі для виявлення MSI з гістології, але дослідники намагаються використовувати штучний інтелект для прогнозування MSI з гістології.
Крім того, HNPCC можна розділити на синдром Лінча I (сімейний рак товстої кишки) та синдром Лінча II (HNPCC, асоційований з іншими видами раку шлунково-кишкового тракту або репродуктивної системи).
Профілактика
Скринінговий тест
Генетичне консультування та генетичне тестування рекомендується сім’ям, які відповідають амстердамським критеріям, бажано до початку раку товстої кишки.
Рак товстої кишки
Колоноскопія рекомендується як профілактичний метод спостереження за особами, які мають синдром Лінча або гени, асоційовані з LS. Зокрема, рекомендується починати колоноскопію у віці 20–25 років для носіїв мутацій MLH1 та MSH2 та 35 років для носіїв мутацій MSH6 та PMS2. Потім колоноскопічне спостереження слід проводити через 1-2 роки для пацієнтів із синдромом Лінча.
Рак ендометрія / яєчників
Для скринінгу раку яєчників та ендометрію щорічно рекомендується трансвагінальне ультразвукове дослідження з біопсією ендометрію або без нього. Для жінок із синдромом Лінча щорічний аналіз крові CA-125 може бути використаний для скринінгу на рак яєчників, однак дані про ефективність цього тесту для зменшення смертності обмежені.
Інші види раку
Існують також стратегії раннього виявлення інших видів раку або зменшення шансів на їх розвиток, які люди з синдромом Лінча можуть обговорити зі своїм лікарем, проте їх ефективність не ясна. Ці варіанти включають:
- Верхні ендоскопії для виявлення раку шлунка та тонкої кишки кожні 3–5 років, починаючи з самого раннього 30 років (бажано в дослідницьких умовах)
- Щорічний аналіз сечі для виявлення раку сечового міхура, починаючи не раніше 30 років (бажано в дослідницьких умовах)
- Щорічні фізикальні та неврологічні обстеження для виявлення раку в центральній нервовій системі (мозку або спинному мозку), починаючи з самого раннього віку 25 років
Критерії Амстердама
Нижче наведено амстердамські критерії при визначенні кандидатів високого ризику для молекулярно-генетичного тестування:
Критерії Амстердама I (всі пункти, що містяться в статті):
- Три або більше членів сім’ї з підтвердженим діагнозом колоректального раку, один з яких є родичем першого ступеня (батьки, дитина, брат або сестра) родичем інших двох
- Два послідовно постраждалих покоління
- Один або кілька раків товстої кишки, діагностовані у віці до 50 років
- Сімейний аденоматозний поліпоз (FAP) був виключений
Критерії Amsterdam II були розроблені в 1999 році та покращили діагностичну чутливість до синдрому Лінча шляхом включення раку ендометрія, тонкої кишки, сечоводу та ниркової миски.
Амстердамські критерії II (всі пункти, що містяться в статті):
- Три або більше членів сім’ї з раком, пов’язаним з HNPCC, один з яких є родичем першого ступеня з двома іншими
- Два послідовно постраждалих покоління
- Один або кілька раків, пов’язаних з HNPCC, діагностовані у віці до 50 років
- Сімейний аденоматозний поліпоз (FAP) був виключений
Хірургія
Профілактична гістеректомія та сальпінгоофоректомія (видалення матки, маткових труб та яєчників для запобігання розвитку раку) можуть проводитися до того, як розвинеться рак яєчників або ендометрія.
Лікування синдрому Лінча
Хірургія залишається першочерговою терапією для HNPCC. Пацієнти з синдромом Лінча, у яких розвивається колоректальний рак, можуть лікуватися або частковою колектомією, або тотальною колектомією з ілеоректальним анастомозом. Через підвищений ризик колоректального раку після часткової колектомії та подібну якість життя після обох операцій, тотальне колектомія може бути найкращим лікуванням HNPCC, особливо у молодих пацієнтів.
Триває суперечка щодо переваг ад’ювантної терапії на основі 5-фторурацилу для колоректальних пухлин, пов’язаних з HNPCC, особливо тих, що перебувають на I та II стадіях.
- Терапія антитілами до PD-1 може бути ефективною.
Блокування контрольної точки за допомогою терапії анти-PD-1 зараз є кращою терапією першого ряду для прогресуючої мікросупутникової нестабільності – високий колоректальний рак.
.

Discussion about this post